Omdat in een reactie de atomen niet veranderen, blijft de totale massa ook gelijk. Dit heet de wet van behoud van massa, of ook de wet van Lavoisier: De producten van een reactie hebben dezelfde massa als de reagentia.
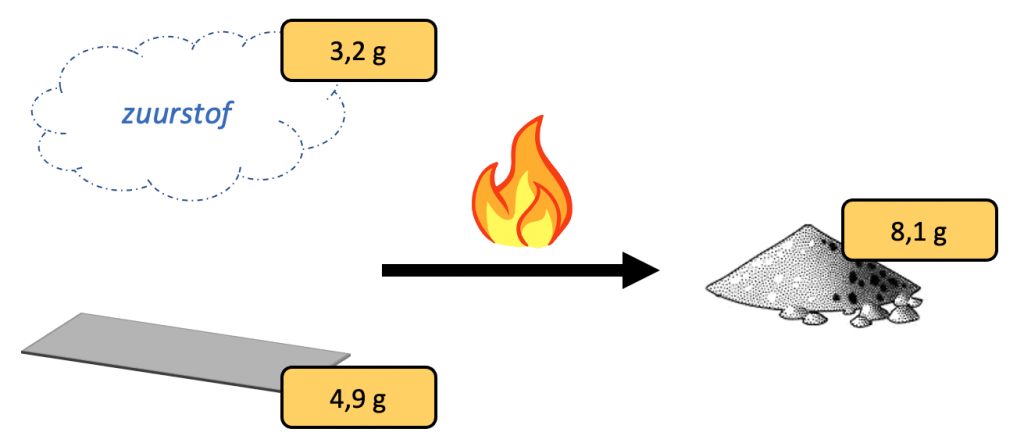
Voorbeeld: Wanneer men 4,9 g magnesium verbrandt, blijft er een wit poeder achter. Dit poeder blijkt een massa te hebben van 8,1 g. Dit lijkt vreemd: hoe kan de massa toenemen?
Men moet echter beseffen dat er zuurstof betrokken was in de verbranding:
$$\mathrm{2\ Mg\ (s) + O_2\ (g) \to 2\ MgO\ (s)}.$$
Nauwkeurige metingen laten zien dat er 3,2 g zuurstof verbruikt werd. Er wordt voldaan aan de wet van behoud van massa, want 4,9 g + 3,2 g = 8,1 g.